Validation de la stérilité dans les emballages RTU
La validation de la stérilité des emballages RTU est essentielle pour comprendre la conception du processus de stérilisation et son impact. Il est important de comprendre que la stérilité est une question de probabilités plutôt que de valeurs absolues. En d'autres termes, quelle est la probabilité qu'un objet stérilisé contienne des organismes survivants et quelles sont les conséquences de cette garantie pour le "produit", par exemple des niveaux dangereux de résidus d'agents stérilisants et/ou des effets néfastes sur les matériaux d'emballage ?
La définition de la stérilité
La stérilité est quantifiée par le Sterility Assurance Level (SAL), qui indique qu'un produit a été rendu stérile. Un SAL de 10-6, par exemple, est le niveau requis par la FDA américaine pour les dispositifs médicaux et les injections, selon la définition d'une approche "overkill". Selon l'USP, la stérilisation " overkill " peut être définie comme une méthode dans laquelle la destruction d'une forte concentration d'un micro-organisme résistant soutient la destruction d'une charge biologique raisonnablement anticipée présente dans le traitement de routine. Il incombe au fabricant de composants "stériles" de surveiller la charge biologique et d'en déterminer les tendances.
Le SAL est déterminé en soumettant le cycle de stérilisation à des niveaux élevés d'organismes résistants et en quantifiant le nombre d'unités formatrices de colonies (UFC) survivantes après la stérilisation. Dans un processus non contrôlé, il y a généralement une grande variation dans la nature et le nombre d'UFC sur le produit tel qu'il est présenté au cycle de stérilisation. La variation est déterminée en contrôlant le(s) produit(s) avant la stérilisation pour les niveaux de charge biologique et la spéciation des isolats (identification de l'organisme) afin de déterminer la résistance inhérente à la modalité de stérilisation. Les surfaces mariées, où deux matériaux s'emboîtent étroitement (comme la protection de l'aiguille et le moyeu de la seringue), et les petites lumières (passages étroits tels que l'intérieur d'une aiguille de petit calibre), représentent des défis importants pour "démontrer" que l'agent stérilisant éliminera avec succès les biocontaminants dans ces endroits difficiles d'accès.
Validation du Stérilité dans l'emballage RTU : les conséquences d'une charge biologique élevée
Si les programmes de surveillance et d'analyse des tendances déterminent que le "produit" contient des niveaux élevés de charge microbienne, des niveaux élevés de variation de la charge microbienne ou des niveaux élevés de résistance, la réglementation exige que les fabricants se penchent sur les processus en amont, par exemple les programmes de nettoyage, la fréquence de nettoyage, la propreté microbiologique des matériaux d'emballage et les processus d'assemblage, ainsi que la sélection et la rotation des agents antimicrobiens. Si la charge microbienne n'est pas maîtrisée, il peut être nécessaire d'ajuster le cycle de stérilisation pour atténuer le risque supplémentaire.
Au fur et à mesure que le produit est soumis à des conditions de stérilisation, la charge biologique inhérente est progressivement éliminée et le nombre d'organismes survivants est réduit et, espérons-le, éliminé. Après un certain temps et dans les bonnes conditions (température, pression, humidité, durée et concentration de gaz), la probabilité de survie atteindra une réduction de spores de 10-6, ce qui signifie qu'il y a une chance incroyablement faible qu'un seul organisme viable survive au cycle de stérilisation.

Des dispositifs de contestation de processus externes (EPCD) contenant des indicateurs biologiques certifiés (BI) contenant >1x106 endospores bactériennes hautement résistantes (vérifiées pour chaque lot par des tests de vérification de la population) sont placés sur chaque palette dans chaque cycle. Après le cycle, les indicateurs biologiques sont retirés et transférés dans un milieu favorisant la croissance. Après incubation, s'il n'y a pas de croissance, vous pouvez être sûr que le cycle de stérilisation a atteint le SAL requis. Ceci, ainsi que l'examen paramétrique de l'enregistrement du traitement du cycle, nous donne l'assurance que le cycle de stérilisation a été exécuté avec succès selon les paramètres validés.
Note : Les indicateurs biologiques sont disponibles à différentes concentrations SAL, préparés à partir de différents organismes, avec différentes résistances inhérentes, pour tester différentes modalités de stérilisation (chaleur, vapeur, EtO, faisceau d'électrons, VHP, H2O2 et Gamma).
Un composant stérile maintiendra la stérilité tout au long de la chaîne de valeur grâce à l'utilisation de processus validés et d'emballages primaires et secondaires conçus de manière appropriée.
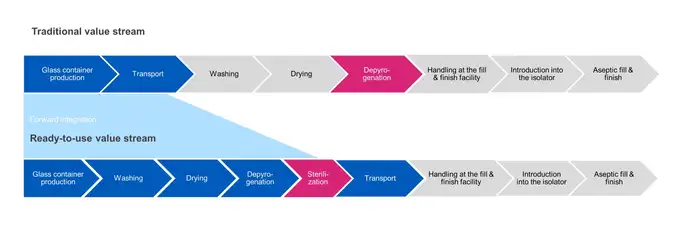
Dans le remplissage en vrac traditionnel, la stérilisation du contenant est effectuée lors de l'étape de dépyrogénation. Les produits sont lavés, séchés puis passés dans un tunnel thermique pour les dépyrogéner à des températures élevées (280-350 °C) afin de garantir leur stérilité avant d'être transférés directement vers l'opération de remplissage.
En revanche, la stérilisation des conteneurs RTU est effectuée après l'emballage pharmaceutique final et avant le transport vers l'installation Fill-and-Finish aseptique. Au cours des étapes suivantes du processus, l'emballage extérieur est retiré et l'emballage intérieur scellé est transféré de manière aseptique dans l'opération de remplissage. Le maintien de la stérilité entre le point de sortie de la chambre de stérilisation et le point d'entrée dans un isolateur aseptique pose des problèmes.
En bref, la stérilité est une question de probabilités, le risque de survie d'organismes sur un objet devant être minimisé par des processus validés et des solutions d'emballage qualifiées. Pour les emballages RTU, la stérilité doit être assurée du point de stérilisation jusqu'à l'isolateur aseptique.
Les emballages primaires RTU de SCHOTT Pharma
SCHOTT iQ® est une plateforme globale qui permet de standardiser les composants des emballages prêts à l'emploi (RTU) et d'améliorer la qualité des conteneurs RTU. Avec SCHOTT iQ®, le développement et l'administration de médicaments injectables de haute qualité deviennent efficaces et améliorent de manière significative la sécurité des patients.
Les variantes disponibles au sein de la plateforme SCHOTT iQ® sont adaptiQ®, syriQ® et cartriQ®, qui sont toutes conditionnées dans des tubes standardisés.
Valider et maintenir la stérilité_accordion_FAQ-01

Dr. Robert Lindner
Product Manager Bulk & Sterile Solutions
Inscrivez-vous pour recevoir les dernières actualités
Tenez-vous au courant des informations sur les produits et services pharmaceutiques SCHOTT et inscrivez-vous à notre newsletter.