Préparation de la soumission de médicament
CONTACTEZ-NOUSNaviguer dans les complexités de la préparation des demandes de soumission de médicaments pharmaceutiques
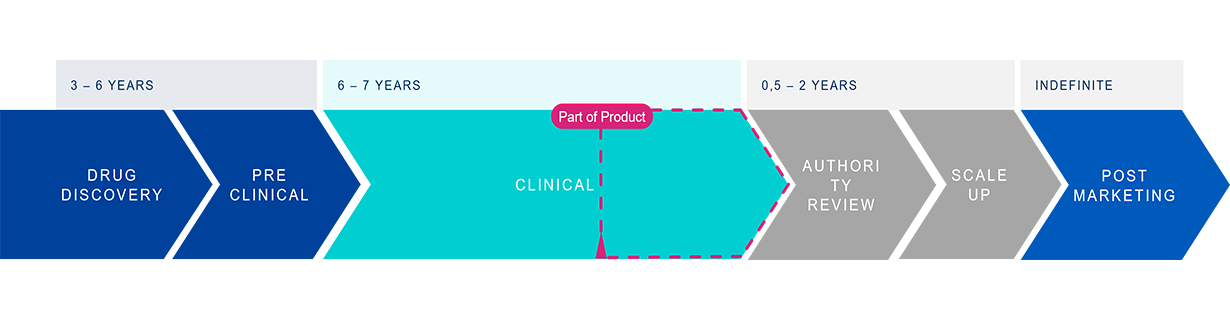
La préparation à l'approbation réglementaire de nouveaux médicaments nécessite des tests approfondis sur l'emballage afin de garantir la sécurité et l'efficacité du médicament. Ces tests couvrent un large éventail d'évaluations, notamment la caractérisation des matériaux, l’interaction médicamenteuse, l'intégrité de la fermeture du contenant et les performances fonctionnelles. Ces tests complets sont essentiels non seulement pour répondre aux normes pharmaceutiques réglementaires strictes, mais également pour garantir la sécurité des patients.
Rationalisation des processus de test pour la conformité réglementaire et la soumission accélérée
Les sociétés pharmaceutiques sont souvent confrontées à des défis dans leur processus de soumission de médicaments, en équilibrant les équipes internes et les laboratoires externes pour leurs besoins de tests. Bien que les équipes internes soient profondément impliquées dans le développement, elles peuvent manquer d'expertise dans certaines procédures de test spécifiques. D'un autre côté, les laboratoires externes offrent des connaissances spécialisées pour les méthodes de test, mais posent souvent des problèmes de coordination et d'intégration des résultats, ce qui conduit à un processus fragmenté avec des résultats incohérents.
Faire face aux pénuries de ressources internes et gérer les fournisseurs externes devient un risque d'échec de la mise sur le marché rapide. Compte tenu de la complexité et des enjeux élevés impliqués dans la phase de préparation de la soumission de médicament, les sociétés pharmaceutiques assument une responsabilité importante, en veillant à ce que le plus haut degré de sécurité des patients soit atteint dans les délais les plus serrés.
Quatre tests pour préparer votre dossier de demande de médicament
Les tests de compatibilité des matériaux sont essentiels pour garantir que les matériaux candidats sont qualifiés pour être utilisés dans l'application de conditionnement de médicaments. Les tests de compatibilité des matériaux servent à :
- Respecter les exigences réglementaires – garantir la conformité aux normes mondiales relatives à l'utilisation des matériaux dans les emballages pharmaceutiques.
- Correspond aux spécifications prévues – confirme les paramètres tels que la composition chimique et l'épaisseur de la couche (par exemple, silicone ou autres revêtements).
Cela implique une évaluation rigoureuse des caractéristiques matérielles des composants d'emballage primaire en verre, en polymère ou en élastomère.
Les procédures de test comprennent :
- Contrôle de conformité – essais standardisés visant à garantir la conformité du matériel aux exigences définies dans les pharmacopées.
- Caractérisation des composants de l'emballage – les tests incluent la mesure de l'épaisseur de la couche ou l'évaluation de la quantité totale ou facilement amovible de silicone.
- Analyse des particules – caractérise la propreté des matériaux et révèle les sources de contamination potentielle provenant de la fabrication.
L'interaction médicamenteuse avec la solution de conditionnement constitue un risque critique pour l'efficacité du médicament. Une évaluation appropriée permet de vérifier la compatibilité de la formule du médicament avec les matériaux de contact du système. Les tests d'interaction médicamenteuse servent à :
- Assurer l'efficacité du médicament – vérifier que le contenant n'altère pas les effets thérapeutiques du médicament.
- Assurer un stockage sûr – confirmer l'absence de sous–produits toxiques critiques provenant de l'interaction médicament-contenant pendant le stockage.
Les tests d'interaction médicament-contenant impliquent une analyse détaillée de la manière dont le médicament interagit avec le contenant, prédisant les changements chimiques et physiques potentiels pendant la durée de stockage. Les méthodes de test comprennent :
- Études de délaminage – évalue le risque de dégradation du matériau et son impact sur le médicament.
- Analyse des particules – compte et caractérise les particules résultant de l'interaction médicament–contenant.
- Études sur les substances extractibles – évalue les produits chimiques potentiels qui pourraient s'échapper du contenant.
- Études sur les substances lixiviables – étudient l'impact des substances lixiviables sur la stabilité des médicaments et la sécurité des patients.
- Analyse des impuretés élémentaires – garantit qu'aucun élément nocif n'est présent dans l'emballage.
L'intégrité de la fermeture du contenant est essentielle pour préserver la stérilité et la qualité d'un produit pharmaceutique tout au long de sa durée de vie. Des tests appropriés permettent d'évaluer le risque de fuite de l'emballage d'un produit pharmaceutique. Le CCIT sert à :
- Assurer l'efficacité et la sécurité des médicaments – il vérifie la conception du système pour soutenir la stérilité et la stabilité d'un produit pharmaceutique.
- Preuve de conformité réglementaire : elle est conforme aux normes mondiales, notamment aux directives de la FDA et de l'EMA.
- Confirme une conception robuste – elle prouve son efficacité contre la contamination et les atteintes à l'intégrité.
Le CCIT garantit que les contenants tels que les flacons et les seringues sont imperméables aux contaminants, ce qui constitue un aspect essentiel de la sécurité des patients et de l'efficacité des médicaments. Le CCIT comprend les tests suivants :
- Test de pénétration de colorant – identifie les fuites microscopiques dans les joints des conteneurs pour vérifier l'intégrité du joint.
- Analyse de l'espace de tête – évalue le changement de la composition du gaz dans les conteneurs scellés au fil du temps pour déterminer la capacité du gaz à pénétrer dans le système de fermeture du conteneur.
Les tests fonctionnels permettent de valider la conception d'un produit afin de répondre aux exigences spécifiques de l'utilisateur et aux normes pharmaceutiques réglementaires. Les tests fonctionnels servent à :
- Assurer les performances – il valide la fiabilité opérationnelle et l'efficacité du conteneur.
- Assurez la conformité du système : il répond aux réglementations strictes de l'industrie et de la sécurité.
Ce groupe de tests valide la conception du système en garantissant une fonctionnalité fiable dans les conditions spécifiques d'utilisation prévue et pendant toute la durée de vie du produit. Cela est particulièrement pertinent pour les produits combinés tels que les médicaments dans des seringues pré-remplies ou des dispositifs d'injection. Les méthodes de test typiques caractérisent le système pour :
- Force de rupture et de glissement – évalue la facilité de distribution.
- Volume livrable et résiduel – pour un dosage précis et un gaspillage minimal.
- Fuite de liquide – assure l'intégrité du conteneur dans diverses conditions.
- Rescellabilité du septum – valide la capacité de la fermeture à se resceller après la pénétration.
- Résistance à la rupture de la bride et du cône Luer – teste la résistance mécanique contre la rupture.
PartnerLab de SCHOTT Pharma : tests pharmaceutiques pour soumission réglementaire
Il est essentiel de comprendre l'importance et la complexité du processus de soumission réglementaire de l'industrie pharmaceutique. Doté de professionnels expérimentés, notre laboratoire de pointe, agréé par la FDA, simplifie et rationalise ce processus. Avec PartnerLab, nous proposons une gamme complète de services de test conçus pour répondre aux exigences diverses et rigoureuses des tests d'interaction et d'emballage des produits pharmaceutiques.Au-delà des tests, nous faisons équipe avec vous pour garantir la sécurité et le succès de votre produit. En nous confiant les complexités des tests et de la conformité, vous pouvez vous concentrer sur vos points forts, en étant sûr que vos tests de performance sont gérés de manière experte. PartnerLab rationalise votre processus de test, accélère votre soumission sur le marché et renforce l'assurance de la qualité et de la sécurité de votre produit.