Preparación para registro del fármaco
CONTÁCTENOSNavegar por las complejidades de la preparación para el registro de medicamentos farmacéuticos
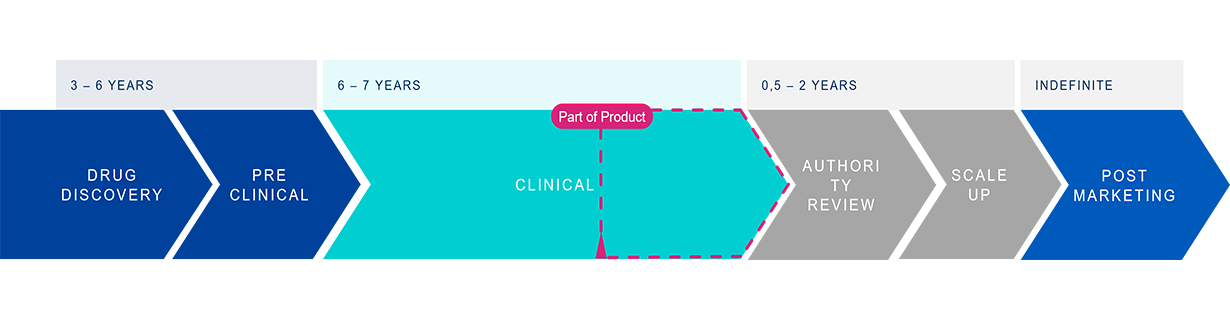
La preparación para la aprobación reglamentaria de nuevos productos farmacéuticos requiere pruebas exhaustivas relacionadas con el envasado para garantizar la seguridad y la eficacia de los medicamentos. Estas pruebas abarcan una amplia gama de evaluaciones, incluida la caracterización de materiales, la interacción entre el envase del fármaco y el envase, la integridad del cierre del envase y el rendimiento funcional. Estas pruebas exhaustivas son esenciales no solo para cumplir con los estrictos estándares normativos, sino también para salvaguardar la seguridad del paciente.
Optimización de los procesos de pruebas para el cumplimiento normativo y la presentación acelerada
Las empresas farmacéuticas a menudo se enfrentan a retos en su proceso de registro de medicamentos, equilibrando equipos internos y laboratorios externos para sus necesidades de pruebas. Aunque los equipos internos están profundamente involucrados en el desarrollo, pueden carecer de experiencia en algunos procedimientos de prueba específicos. Por otro lado, los laboratorios externos ofrecen conocimientos especializados para los métodos de comprobación, pero a menudo plantean retos de coordinación e integración de resultados, lo que conduce a un proceso fragmentado con resultados inconsistentes.
La gestión de la escasez de recursos internos y la gestión de proveedores externos se convierten en un riesgo de fracaso en el rápido tiempo de comercialización. Con la complejidad y los altos niveles de interés involucrados en la fase de preparación de la presentación, las empresas farmacéuticas deben asumir una responsabilidad significativa a la hora de garantizar que se logre el máximo grado de seguridad del paciente con las restricciones de tiempo más estrictas.
Cuatro pruebas para la preparación de registro de medicamentos
Las pruebas de compatibilidad de materiales son fundamentales para garantizar que los materiales candidatos estén cualificados para su uso en la aplicación de contención de fármacos. Las pruebas de compatibilidad de materiales sirven para:
- Cumplir los requisitos normativos: garantizar la conformidad con los estándares globales para el uso de materiales en el envasado farmacéutico.
- Corresponde a la especificación prevista: confirma parámetros como la composición química y la espesura de la capa (por ejemplo, silicona u otros recubrimientos).
Esto implica una evaluación rigurosa de las características del material del vidrio, polímero o componentes del envase primario elastomérico. Los procedimientos de prueba incluyen:
- Pruebas compendiales: estandarizadas para garantizar la conformidad de los materiales con los requisitos definidos en las farmacopeas.
- Caracterización de los componentes del envase: las pruebas incluyen la medición de la espesura de la capa o la evaluación de la cantidad total o fácilmente extraíble de silicona.
- Análisis de partículas:caracteriza la limpieza de los materiales y revela las fuentes de contaminación potencial de la fabricación.
La interacción del fármaco con la solución de contención es un riesgo crítico para la eficacia del fármaco. Una evaluación adecuada verifica la compatibilidad de la fórmula del fármaco con los materiales de contacto del sistema. Las pruebas de interacción farmacológica sirven para:
- Garantizar la eficacia del fármaco: verificar que el envase no altere los efectos terapéuticos del fármaco.
- Garantice un almacenamiento seguro, confirmando la ausencia de subproductos tóxicos críticos de la interacción entre el medicamento y el envase durante el almacenamiento.
Las pruebas de interacción fármaco-envase implican un análisis detallado de cómo interactúa el fármaco con el envase, prediciendo posibles cambios químicos y físicos durante el tiempo de almacenamiento. Los métodos de prueba incluyen:
- Estudios de delaminación: evalúa el riesgo de degradación del material y su impacto en el fármaco.
- Análisis de partículas: cuenta y caracteriza las partículas resultantes de la interacción entre el envase del fármaco.
- Estudios de sustancias extraíbles: evalúa los productos químicos potenciales que podrían lixiviarse del contenedor.
- Estudios de lixiviables: investiga el impacto de los lixiviables en la estabilidad de los fármacos y la seguridad de los pacientes.
- Análisis de impurezas elementales: garantiza la ausencia de elementos nocivos en el envase.
La integridad del cierre eficaz del envase es fundamental para salvaguardar la esterilidad y la calidad de un producto farmacéutico durante toda su vida útil. Las pruebas adecuadas permiten evaluar el riesgo de fugas en el envase de un producto farmacéutico. CCIT sirve para:
- Garantizar la eficacia y la seguridad de los fármacos: verifica el diseño del sistema para respaldar la esterilidad y la estabilidad de un producto farmacéutico.
- Prueba de conformidad con las normativas: se ajusta a los estándares globales, incluidas las directrices de la FDA y la EMA.
- Confirma un diseño robusto: demuestra eficacia contra la contaminación y las infracciones de integridad.
CCIT garantiza que los contenedores, como viales y jeringas, sean impermeables a los contaminantes, lo que es un aspecto vital de la seguridad del paciente y la eficacia del fármaco. El CCIT incluye las siguientes pruebas:
- Prueba de penetración de tinte: identifica fugas microscópicas en los sellos de los contenedores para verificar la integridad del sellado.
- Análisis del espacio libre: evalúa el cambio en la composición del gas dentro de los contenedores sellados a lo largo del tiempo para determinar la capacidad del gas para permear el sistema de cierre del contenedor.
Las pruebas funcionales validan el diseño de un producto para satisfacer los requisitos de usuario específicos de la aplicación y los estándares normativos. La prueba funcional sirve para:
- Garantizar el rendimiento: valida la fiabilidad y eficacia operativa del contenedor.
- Garantizar la conformidad del sistema: cumple con las estrictas normativas de la industria y de seguridad.
Este grupo de pruebas valida el diseño del sistema para proporcionar una funcionalidad fiable en las condiciones específicas del uso previsto y durante toda la vida útil del producto. Esto es especialmente relevante para productos combinados, como fármacos en jeringas precargadas o dispositivos de inyección. Los métodos de prueba típicos caracterizan el sistema para:
- Fuerza de rotura y deslizamiento: evalúa la facilidad de dosificación.
- Volumen suministrable y residual: para una dosificación precisa y un desperdicio mínimo.
- Fuga de líquido: garantiza la integridad del contenedor en una variedad de condiciones.
- Resellabilidad del tabique: valida la capacidad del cierre para volver a sellar después de la penetración.
- Resistencia a la rotura de la brida y el cono Luer: prueba la resistencia mecánica a la rotura.
PartnerLab de SCHOTT Pharma: Pruebas farmacéuticas para el registro normativo
Comprender la importancia y la complejidad del proceso de registro normativo de la industria farmacéutica es clave. Nuestro laboratorio de última generación, registrado por la FDA y dotado de personal experto, simplifica y agiliza este proceso. Con PartnerLab, ofrecemos un conjunto completo de servicios de pruebas diseñados para satisfacer los diversos y estrictos requisitos de los envases de productos farmacéuticos y las pruebas de interacción.Más allá de las pruebas, nos asociamos con usted para garantizar la seguridad y el éxito de su producto. Al confiarnos las complejidades de las pruebas y el cumplimiento, puede centrarse en sus puntos fuertes principales, con la confianza de que sus pruebas de rendimiento se gestionan de forma experta. PartnerLab agiliza su proceso de pruebas, acelera su sumisión al mercado y aumenta la garantía de la calidad y la seguridad de su producto.