Implicações na transição de vacinas mRNA contra a Covid-19 do frasco para a seringa pronta para envasar
Apesar das novas variantes, a pandemia da Covid-19 inevitavelmente evoluirá para uma situação endêmica. Em muitos países ocidentais, 70-90 % da população foi vacinada – um feito sem precedentes que não poderia ter acontecido sem centros de vacinação em massa. O recipiente ideal para a vacina foi o frasco multidose, que oferece uma rápida comercialização respaldada por uma vasta experiência em envase e acabamento, além de conhecimento em regulamentação.
Da pandemia à endemia
Quando a doença se torna uma endemia, o controle consiste em novas vacinações periódicas, especialmente para pacientes de alto risco. Isso é mais provável de ocorrer em unidades de saúde locais, onde o frasco multidose atual pode não ser a solução mais eficiente. Isso porque, assim que o frasco é aberto, a validade da vacina é uma questão de horas e todas as doses não utilizadas devem ser descartadas.
Mudar de um frasco multidose para um de dose única ou uma seringa pronta para o envase (PFS) feita de polímero ou vidro melhoraria a usabilidade e reduziria o desperdício, mas há muitas perguntas que precisam ser respondidas. Uma PFS é um dispositivo complexo com múltiplos componentes, todos os quais podem ser afetados pela exigência de transporte aéreo a uma pressão atmosférica reduzida, bem como ciclos de congelamento/descongelamento e o armazenamento em temperatura extremamente baixa exigido pelas vacinas de mRNA.
Portanto, a SCHOTT Pharma configurou um programa de testes elaborado usando seringas SCHOTT TOPPAC® de 1 ml/1 g feitas de copolímero de olefina cíclica (COC), introduzindo uma série de variáveis para obter uma melhor compreensão dos parâmetros críticos. As seringas foram preenchidas com água para injeção (WFI) ou placebo de sacarose e congeladas durante um ou dois ciclos a -20 °C, -50 °C e -80 °C. Três êmbolos diferentes foram usados: borracha de halobutila padrão, um êmbolo parcialmente laminado e um êmbolo laminado otimizado para forças de deslizamento. Os volumes de envase foram de 0,25 ml, 0,5 ml, 0,75 ml e 1 ml, e o espaço livre foi de 2 mm, 4 mm ou 6 mm. As seringas foram submetidas à pressão atmosférica normal, bem como à simulação de transporte aéreo.
Movimento do êmbolo
A primeira pergunta abordada é sobre os efeitos da barreira estéril, que pode ser rompida pelo movimento excessivo do êmbolo. Três fatores influenciam o movimento do êmbolo: a quantidade de espaço livre, o volume de envase e o tipo de êmbolo. Diferentes temperaturas de congelamento e meios de envase foram testados, mas nenhuma diferença foi observada.
O movimento do êmbolo é sempre o mais crítico durante a simulação de transporte (baixa pressão), mas escolher o tipo certo de êmbolo e otimizar o processo de envase e acabamento pode controlar isso e garantir que a barreira estéril não seja violada.
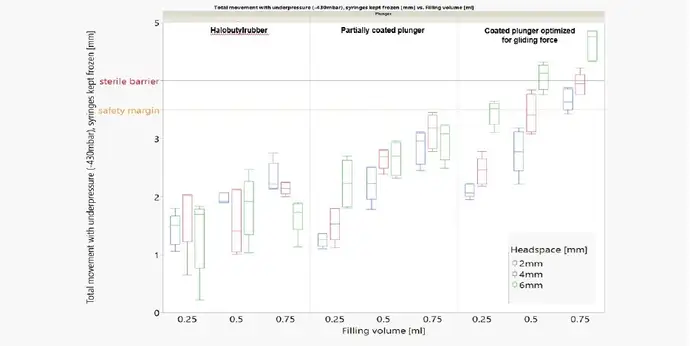
Comparação do desempenho de seringas com êmbolo de borracha de halobutil padrão, êmbolo parcialmente laminado e êmbolo laminado
Funcionalidade
O próximo desafio é a funcionalidade, especialmente os efeitos sobre a força de liberação do êmbolo (BLF) e sobre as forças de deslizamento (GF) de diferentes temperaturas ao longo de múltiplos ciclos de congelamento/descongelamento. Ao longo de três ciclos de congelamento/descongelamento, não houve diferença significativa entre seringas vazias ou cheias.
Dando um passo além, a SCHOTT Pharma investigou uma temperatura ainda mais baixa de -50 °C usando três tipos de êmbolos diferentes: borracha de halobutil, parcialmente revestida e revestimento de êmbolo otimizado para força de deslizamento. Novamente, quase não houve diferença entre -20 °C e -80 °C para GF e BLF.
Siliconização
Outro desafio é a siliconização. As seringas precisam ter uma camada de lubrificação dentro do cilindro para possibilitar o movimento do êmbolo, mas o excesso de óleo de silicone livre pode criar gotículas dentro da seringa capazes de reagir com o medicamento, tornando-o instável.
A SCHOTT Pharma testou duas tecnologias diferentes de siliconização nas seringas SCHOTT TOPPAC®: siliconização reticulada, padrão na SCHOTT TOPPAC®, e a tecnologia de siliconização pulverizada. Dois grupos de cinco seringas, cada qual usando uma dessas tecnologias, foram abastecidas com WFI e armazenadas/congeladas em diferentes temperaturas antes do extrato ser agrupado e analisado através de absorção atômica para óleo de silicone livre.
A -5 °C e -20 °C, o silicone pulverizado resultou em silicone muito mais extraível do que a siliconização reticulada: 5 vezes maior e 24 vezes maior, respectivamente. Isso demonstrou que os ciclos de congelamento/descongelamento têm um efeito significativo nas seringas com óleo de silicone pulverizado.
A tecnologia de siliconização tem um impacto ainda maior sobre partículas subvisuais (>10 μm) em temperaturas de congelamento, com temperaturas mais baixas parecendo aumentar a carga de partículas.
De modo similar, a tecnologia de siliconização também tem um impacto significativo na contagem de partículas, com a camada de silicone imobilizada da siliconização reticulada proporcionando o nível mais baixo de partícula. Nas mesmas condições, seringas sem silicone não apresentaram partículas; portanto, há uma alta probabilidade de que todas as partículas subvisuais observadas tenham se originado da siliconização.
Integridade do fechamento do recipiente
A integridade do fechamento/recipiente também pode ser afetada por temperaturas extremamente baixas, como -80 °C, devido à perda de elasticidade nos componentes de borracha e às variadas taxas de encolhimento de diferentes materiais. Por exemplo, não é incomum ver que o cilindro da seringa encolhe muito menos que o êmbolo, o que poderia resultar em sobreposição mínima e em uma violação da barreira contra a entrada biológica.
Foram realizados testes nas seringas SCHOTT TOPPAC® de 1 mL/1 g com componentes de borracha de halobutilo padrão para protetor de ponta e êmbolo, e comparados com uma variedade de amostras de controle. Os resultados mostraram que mesmo a -80 °C não houve entrada de CO2 após 24 horas.
A estabilidade mecânica e as propriedades ópticas também não foram afetadas pelo armazenamento em temperaturas muito baixas, sem aumento de quebra ou rachaduras por estresse, e sem desgaste ou defeitos visuais adicionais.

Solução ideal
A SCHOTT Pharma investiga continuamente as variáveis de produtos e processos para ajudar os fabricantes de mRNA em busca da embalagem primária ideal. Isso inclui possíveis interações entre o fármaco e o recipiente resultantes de extraíveis e lixiviáveis provenientes do recipiente, e os efeitos do recipiente e das condições de armazenamento na estabilidade das nanopartículas lipídicas usadas como veículo. A empresa também está desenvolvendo um pacote de dados semelhante para seringas de vidro syriQ® prontas para envasar.
Enquanto isso, este amplo pacote de dados mostra que as seringas SCHOTT TOPPAC® são altamente adequadas para vacinas de mRNA.

Christoph Zauner
Head of Product Management Polymer Solutions
Cadastre-se para receber as últimas notícias
Mantenha-se atualizado com as informações sobre os produtos e serviços da SCHOTT Pharma e cadastre-se para receber nosso boletim informativo.